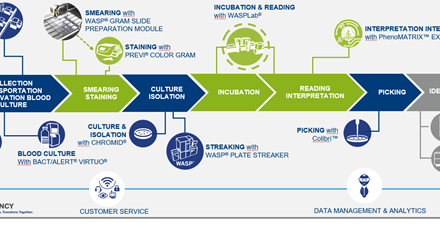
As aprovações regulamentares, como é do conhecimento geral, são uma etapa importante para colocar produtos no mercado. Um dispositivo com marcação CE está dentro dos padrões de segurança necessários estabelecidos pela União Europeia e pode, assim, ser vendido na Europa. Nos EUA, a FDA (Food and Drug Administration) revê os dispositivos clínicos para segurança e eficácia. A aprovação da FDA é, por iss o, um pré-requisito essencial para comercializar um dispositivo médico nos EUA. A bioMérieux tem o prazer de anunciar que os laboratórios na Europa já têm disponíveis três produtos aprovados pela FDA e com marcação CE-IVD:
- Base de dados VITEK® MS V3 (KB) V3.0 atualização de software
- BACT/ALERT® VIRTUO® – aparelho automatizado para deteção de hemoculturas
- RAPIDEC® CARBA NP – para detecção qualitativa de microrganismos produtores de carbapenemase
VITEK® MS V3

Em julho de 2017, o VITEK® MS V3 foi o primeiro Sistema de espectrometria de massa MALDI-TOF1 que recebeu a aprovação FDA 510(k) para a identificação de micobactérias, Nocardia e fungos filamentosos. Estes microrganismos difíceis de identificar requerem habitualmente dias ou mesmo semanas em condições de cultura específicas para um crescimento apropriado, requerendo também testes avançados para identificação ao nível das espécies.
A atualização de software do VITEK® MS, proporciona agora a identificação segura, simples e fiável destes patogéneos em minutos2. Fornece aos clínicos resultados acionáveis para gerir infeções, tais como para a tuberculose, infeções dos ossos e dos pulmões, e outras infeções graves dos órgãos causadas por estes microrganismos. O sistema funciona com kits de extração e de inativação prontos a usar, que também são aprovados pela FDA e com marcação CE. A nova aprovação da FDA expande a base de dados a mais 78 espécies:
- 19 micobactérias incluindo o grupo de Mycobacterium tuberculosis (TB) e as mais frequentes micobactérias não tuberculosas (NTM)
- 12 Nocardia
- 47 bolores, incluindo os clinicamente mais relevantes
A nova base de dados do Sistema VITEK® MS e os kits de reagente estão agora comercialmente disponíveis nos EUA, bem como em países que reconhecem a marcação CE.
BACT/ALERT® VIRTUO®

O Sistema de deteção microbiana de hemoculturas automatizado BACT/ALERT®VIRTUO® recebeu a aprovação FDA 510(k) em Março de 2017, está disponível no mercado dos EUA, e também em países que reconhecem a marcação CE.
O BacT/ALERT® VIRTUO® é o Sistema de deteção microbiana para hemoculturas que lhe oferece a tecnologia “Load & Go”, ajudando os laboratórios a simplificar o seu fluxo de trabalho. Proporciona-lhe novos algoritmos patenteados para deteção precoce de crescimento microbiano. Esta melhoria fornece um tempo mais rápido para a deteção, e por isso, obtém-se uma identificação mais rápida de infeções da corrente sanguínea3,4,5,6,7,8. O BacT/ALERT® VIRTUO® proporciona uma configuração integrada com capacidade de incubação expansível com capacidade para 428 a 1,712 garrafas.
O Sistema funciona com os meios BACT/ALERT® FAN®, que são formulados para otimizar a neutralização do antibiótico com ótimo desempenho dos microrganismos, não obstante de poder utilizar outros meios de cultura BACT/ALERT®. Uma tecnologia única de deteção de nível de sangue que mede o volume de sangue em cada garrafa de hemocultura no momento do carregamento. Isto ajuda os laboratórios a verificar que o volume de sangue recomendado é colhido, fator crucial para detetar infecções da corrente sanguínea.
A deteção mais rápida de patogéneos com VIRTUO® fornece informação crucial para otimizar o tratamento do paciente, especialmente em condições fatais, como a sépsis.
RAPIDEC® CARBA NP
O RAPIDEC® CARBA NP recebeu a aprovação FDA 510(k) em Abril de 2017, e está agora comercialmente disponível nos EUA, bem como em países que reconhecem a marcação CE.
O RAPIDEC® CARBA NP é um teste fenotípico (colorimétrico) que é utilizado para a deteção qualitativa de Enterobacteriaceae e Pseudomonas aeruginosa9 produtoras de carbapenemases . Baseia-se no princípio de teste Carba NP descrito por Nordmann, Poirel e Dortet10, 11.
As Carbapenemases são β-lactamases que são capazes de inactivar a maioria das β-lactames existentes. Espalham-se entre os bacilos Gram-negativos e são um grande problema de saúde pública visto exibirem uma resistência extensiva e espalharem-se rapidamente no mundo inteiro. Há um risco alto de mortalidade para pacientes infetados com estirpes produtoras de carbapenemase. Assim, a deteção rápida é da maior importância para determinar o tratamento apropriado para reduzir o risco de infeção primária e secundária, e para ter a capacidade de implementar medidas de prevenção de infeção para travar o surto nas instituições de cuidados de saúde.
Dr Poirel deu recentemente uma entrevista sobre a resistência à Carbapenemase no ECCMID 2017
Referências bibliográficas:
-
MALDI-TOF : Matrix Assisted Laser Desorption Ionization – Time Of Flight
-
Mather, C.A., et. al. Comparison of the Bruker Biotyper and Vitek MS Matrix-Assisted Laser Desorption Ionization–Time of Flight Mass Spectrometry Systems for Identification of Mycobacteria Using Simplified Protein Extraction Protocols. J. Clin. Microbiol. 2014, 52(1):130.
-
LIOTTI, FM. et. al. “Laboratory Evaluation of the BacT/ALERT® VIRTUO® Automated Blood Culture System”. ECCMID 2016 poster EP0958.
-
MENCHINELLI, F. et. al,. “BacT/ALERT® VIRTUO: a New Automated Colorimetric Microbial Detection System for Detection of Bacteremia”. AMCLI 2015 Poster.
-
MULLIS, D. et al. “Comparison of the bioMérieux Virtuo BacT/Alert Microbial Detection System to the BacT/Alert 3D”. Dublin 2016 Poster.
-
CHAN, Y-J. et. al. “Comparison of the new generation of blood culture system with the BacT/ALERT® 3D system for the detection of bacteremia in patients from emergency room.” ECCMID 2016 Poster.
-
CONGESTRI, F. et. al. “Comparison of ‘time to detection’ values between BacT/ALERT VIRTUO and BacT/ALERT 3D instruments for clinical blood culture samples.” Int. J. Infect. Dis., 2017, vol. 15, n°62, 1-5.
-
ALTUN, O. et. al. “Controlled evaluation of the new BacT/ALERT VIRTUO blood culture system for detection and time to detection of bacteria and yeast.” J. Clin. Microbiol., 2016, vol. 54, n°4, 1148-1151.
-
RAPIDEC® CARBA NP has US FDA clearance for Enterobacteriaceae and Pseudomonas aeruginosa, is CE marked for Enterobacteriaceae, Pseudomonas aeruginosa and Acinetobacter baumannii.
-
NORDMANN P., POIREL L., DORTET L. Rapid detection of carbapenemase-producing Enterobacteriaceae. Emerging Infectious Diseases, www.cdc.gov/eid, 2012, vol. 18, n°9, 1503-1507.
-
DORTET L., POIREL L., NORDMANN P. Rapid identification of carbapenemase types using a biochemical test in Enterobacteriaceae and Pseudomonas. Antimicrobial. Agents Chemother., 2012, vol. 56, n°12, 6437-6440.